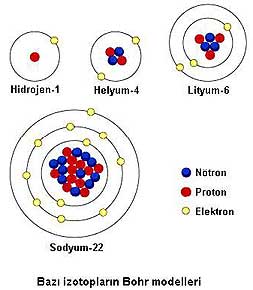
Dış kabuğu dolu olan elementler tepkimeye girmezken, diğerleri dış kabuklarını doldurmak üzere, elektron alıyor veya veriyordu. Model, atom numarasına göre yeniden düzenlenmiş olan elementler tablosundaki periyodiklik açığa kavuşturmuş olmakla beraber; elektronların neden belli enerji düzeylerinde bulunmak zorunda oldukları ve niye sürekli ışıyıp enerji kaybederek çekirdeğe düşmedikleri gibi yanıtlanmamış sorulara, bir yenisini daha eklemişti: Neden birinci kabukta sadece iki ve sonraki kabuklarda sadece 8'er elektron bulunuyordu? Modelde bir şeyler eksikti...